2022年11月29日体験記・寄稿
体験記:カナダ(当院)での治療内視鏡フェローの報告

カナダ・シャルブルック大学 治療内視鏡フェロー 白鳥安利
先生方は内視鏡領域の海外留学についてどのようなイメージをお持ちでしょうか?もしかしたら、北米へ内視鏡留学を考える方はそう多くないかもしれません。理由としては、1) 日本での経験で十分だと感じ、わざわざ留学する必要性が少ない、2) 情報が少ない、3) 入り込むのが難しい、が挙げられると思います。日本の内視鏡技術は世界トップで、素晴らしいものです。私が日本で受けたトレーニングや、これまで参加した画像診断の研究会は濃い内容ばかりでした。一方で、留学で経験した治療内視鏡フェロープログラムや北米独特の手技、現地医師とのネットワークは大変貴重だと感じています。内科レジデンシーの留学情報は潤っているのに対し、内視鏡フェローとして留学する情報は十分と言えず、ご報告させていただきたく思います。
今回、カナダの内視鏡フェローということで紹介させていただきますが、留学先はケベック州のシャルブルック大学 (2021年9月〜2022年11月)になります。プログラム責任者のDr. George Ratebは日本へ留学経験があり、診断学やESDへの造詣も深いです。聖路加国際病院に在籍していた2019年に知り合い、治療内視鏡フェローとして招聘していただくご縁に繋がりました。同大学ではこれまで日本人医師の先例がなく、自分のスタイルを自由に作れるメリットがありました。指導医とフェローという関係ですが、現地の医師達とお互いを尊重し合える関係を築けていると感じます。カナダはアメリカのような国家試験を必須とせず、日本の専門医資格と英語試験でフェローの留学応募が可能です。

George Rateb先生との出会い。左から島村先生、池谷先生、Rateb先生、山本先生、筆者。
1. 治療内視鏡フェローの役割、環境
治療内視鏡フェローの役割は消化管や胆膵を問わず、治療に区分される手技をすべて担います。胆膵内視鏡(EUS、ERCPをそれぞれ年間600件)や消化管ステント、上下部EMRが軸ですが、日本での経験を活かせるよう、それまでほとんど行われていなかったESDを導入し、アドバイザーとしての役割もいただきました。日本でも経験できるこれら治療以外に、北米独特の疾患や手技 (膵嚢胞性疾患の穿刺や食道RFAなど)も実施する機会がありました。他には、院内外の研究会での発表や臨床試験への参加がありました。
朝8時から手技が始まるため、症例の経過や画像、治療プランを事前に予習しておきます。胆膵内視鏡の件数だけでも、日本のハイボリュームセンターが複数の医師で分担する年間件数に相当するのではないかと思います。これだけ多くの処置を第一施行医としてこなすことができるのは、北米独自の医療体制が背景にあります。内視鏡治療は特定の施設に集約されるシステム(ケベック州の場合はMcGill大学、Montreal大学、Sharbrooke大学に地域ごと振り分け)であり、また内視鏡フェローは治療患者以外の病棟業務や外来が免除され、治療に専従します。他施設からの紹介患者は処置後に入院先へ戻り、一般内科や消化器スタッフによる入院管理もしくはホームドクターによる外来フォローを受けます。これは初診外来から治療、入院管理まで同じ医師が対応する日本の医療文化と大きく異なります。そのため、北米の施設にいると一般内科や開業医との垣根がとても低いことを感じます。
また、カナダではカナダ人を診察すると思われるかもしれませんが、実際は多種多様の方を診察します。今回はカナダ人、次はメキシコ人、フランス人、最後はアフリカ出身の方といった具合です。それぞれ人種、傾向のある疾患も違いますので、幅広い対応が身に付きます。こういった多民族性は医療者側にも言え、非英語圏出身のスタッフもおり、純日本人だからと言って言葉の壁に卑屈にならず、努力で順応できると個人的に感じています (ケベック州は英語だけでなく、仏語もメインで使われます)。

シャルブルック大学病院本院

シャルブルックの街の光景
2. 胆膵分野(EUS/ERCP)
胆膵領域に関して、EUS、ERCPともに十分な症例数をこなせること、日本では一般的ではない膵嚢胞性病変への穿刺検査や胃空腸バイパスステント (G-J stent)などのinterventional EUSに関わる機会があることが強みと考えられます。EUSは3名、ERCPは5名の指導医が日々交代で共に検査につくため、各指導医の手持ちのtipsを学べます。手取り足取り内視鏡が安定する身体の使い方を指導する医師や、EUS画像の解説が細かい医師、新しいアイデアで困難症例に挑む医師、最新の文献チェックに余念がない医師など、指導医もタイプ様々です。それぞれの指導医の手技の趣向に併せて、フェローはその都度適応しなければなりませんが、自分にとって良い部分を整理し、独り立ち後にオリジナルの型を目指せば良いと思います。
EUSについて、まず検査そのものの敷居が低く、広く普及している印象を受けました。胆管炎疑いの救急患者に対し、日本はCT、MRCPへの信頼が厚いところですが、こちらでは来院早々にEUSを行い、結石ありとなれば同日ERCPを組むという流れを頻繁に経験しました。感度、特異度ともEUSは優れている報告1-3から、EUSの位置付けが最上位になっているようです。CTで原因がはっきりしない膵炎、胆嚢炎に対しても、ほぼ必ず入院中にEUS評価を行っていました。
処置はEUS-FNAB(縦隔、消化管間葉系腫瘍、肝腫瘍、膵腫瘍、膵嚢胞性疾患)、EUS-CDS(HOT-AXIOSによる経十二指腸胆道ドレナージ)、EUS-HGS(SPAXUS stent)、EUS-PD(plastic stentによる経胃膵管ドレナージ)、EUS-CD(WONのnecrosectomy)、EUS-CPNを中心に行い、G-J stentも6例経験しました。FNAに関しては蓄積された症例データや既報から、1回目は陰圧なしでfanningでの採取、2回目以降でnegative water pressure aspirationが実施されていました4 (検体評価はMOSE)。また日本では播種リスクの懸念からコンセンサスが得られていない膵嚢胞性疾患への穿刺検査は、外科治療かフォローアップか迷った際には日常的に行われ、性状、腫瘍マーカー、アミラーゼ、病理が評価されました。具体的には、worrisome featureを伴うIPMN、増大が目立つSCN、MCNを疑う病変、嚢胞変性のあるpanNETを疑う病変、などが穿刺の対象となり、外科医へのコンサルトに必須となりました。日本での習慣のまま3ヶ月後MRIフォローとコメントし、その場に居合わせた外科医から「それでは外科治療の判断ができないではないか」とお叱りを受けたこともありました。画像診断でIPMNとされていてもMCN (string sign陽性で穿刺直後に診断できたケースがありました)やNETということは10-15%あり5、穿刺して良かったと感じる経験もありました。MRCPも撮影されますが、あくまで時系列評価やダブルチェックとしての位置付けでした。
また、interventional EUSやデバイスの産学共同は、日本より活発な印象がありました。ERCP不成功・施行困難例の胆道閉塞に、経皮的ドレナージが検討されることはほぼなく、EUS下ドレナージが選択されました。また、数例ながら良性膵嚢胞に対するアブレーション治療 (エタノール局注)も経験しました。G-J stentについてはHOT-AXIOSが必須となりますが、標的となる空腸を確実に緊満・描出させるシステムの開発、研究が行われており6、より確実で簡易なモデルの登場が目指されています。
ERCPについては処置、デバイスともあまり日本と差異ないと感じましたが、件数が多いため様々な状況下(術後腸管、クローン病が背景にあり粘膜観察すら困難な症例、巨大傍乳頭憩室、体動困難例など)でのトレーニングが経験できました。pre-cutやSpyglassでのEHL症例も多く施行できました。口側隆起の長い症例でのpre-cutへの移行や、EST後出血に対するmetalic stent留置などの判断は、日本で経験したよりも早いと感じました。
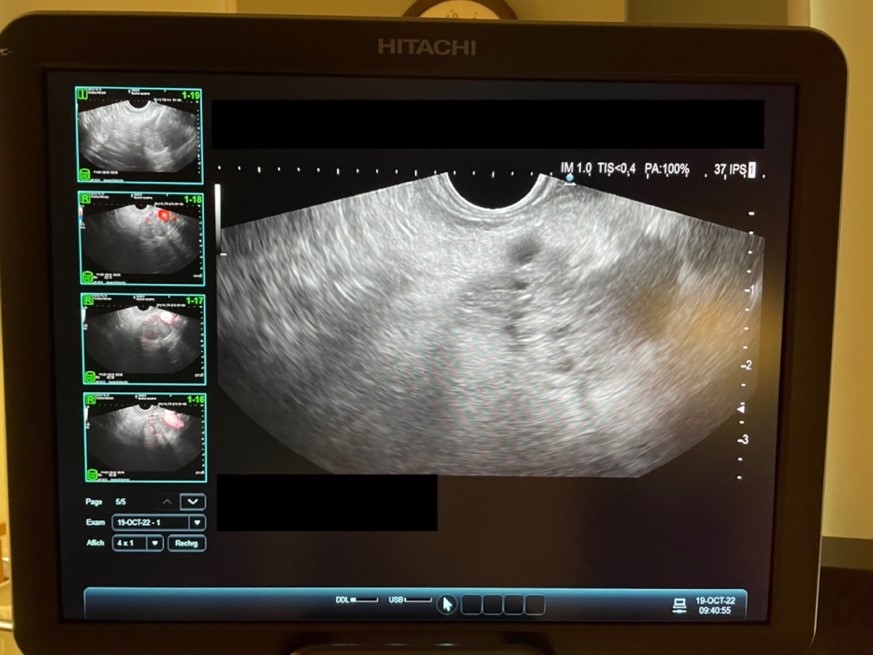
EUS-FNAでpanNETの診断がされた症例
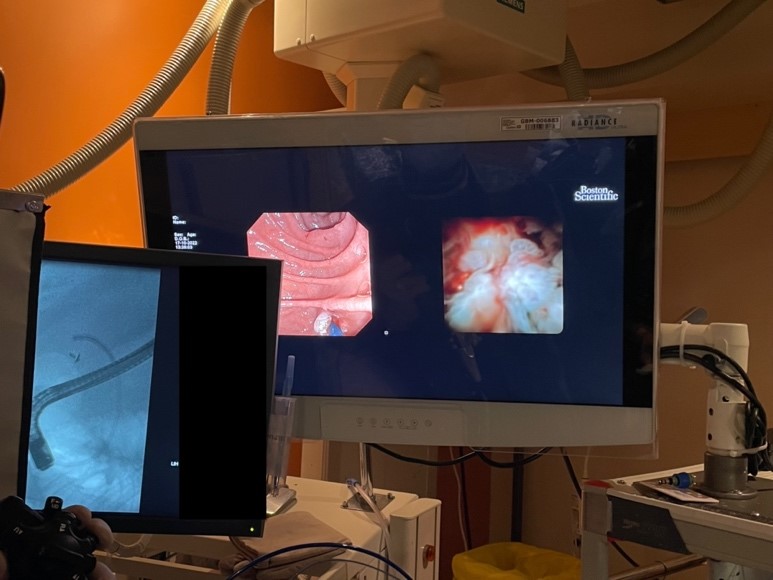
胆道鏡で診断された胆管乳頭種の症例
3. 消化管分野(ESD/食道RFAなど)
ESDはフェロー期間中に計44例経験し、大腸が28例 (右側結腸が7割)、胃が11例 (多くは接合部、体上部病変)、食道が5例 (すべて腺癌)でした。治療用スコープ (GIF-1TH190、PCF-H190L)やナイフ(Dual J)、フード、高周波装置 (VIO300D, VIO3)、局注 (ヒアルロン酸代わりのEleview)は揃えることができ、日本とほぼ同様の環境で治療が行えた印象があります。一方、拡大内視鏡の常備がなく、また紹介医からの情報で画像添付がない場合も多く、当日治療という中で術前の範囲診断に不安を感じる場面が多々ありました。この診断学の粗雑さは北米全体に言える傾向かと思います。胃ESD症例で、せめてdual focus (GIF-HQ190)による評価や陰性生検による病理の裏打ちをして別日に治療した方が良いのでは、という話し合いをしたのを覚えています。ESDはその技術的難易度が北米での普及を遅らせている要因と思われがちですが、それ以上に問題となっているのは、制限された時間内により多くの治療をこなさなければいけない治療内視鏡医の負担 (北米では治療内視鏡医が少ない)、ESDで点数加算がされない保険制度などが挙げられます (ERCPの方が確実に稼ぐことができます)。また、治療困難例に対し、日本では職人芸のようなESD技術が披露されるのに対し、彼らはEMR+焼灼 (処置時間が推測できる)や全層切除してから縫縮しよう(新たなデバイス開発で克服しよう)と検討するような、根本的な考え方の違いがあります。その中でも、北米でESDを行う医師は少しずつ増えてきています。日本でトレーニングを受けた医師など、既にとても上手な内視鏡医もいます。私のような日本人フェローの場合、どうしても言語面で仕事がスムーズにいかないことを経験するため、ESDのアドバイザーなどの役を与えていただくことは、留学先での居心地の良さにつながります。
バレット食道病変について、北米ではdysplasiaや表在癌などの粘膜不整域に対して内視鏡治療 (ESD or EMR-L)を行った後、RFAカテーテル(当院ではBarrx 90 RFAを使用)で背景バレット粘膜の焼灼を行い、扁平上皮化(腸上皮化生の消失)を目指します。現在、日本ではRFAデバイスの使用ができないため、これらの手技は留学でしか得られない経験となっています。なお、RFAデバイスのthrough-the-scope typeはGAVEにも応用可能です。公知であるEGJやLSBE (欧米では全周ではなく最大長>3cm)の定義の違い、バレット粘膜の病理学的定義など、日本と異なる点は認識しておく必要があります(プラハ分類の記載は必須と考えます)。将来的に、日本でもLSBEが増加すればRFAデバイスが必要となる日が来るかもしれません。
POEMに関してはカナダ内のいくつかの施設(トロント、キングストンなど)で行われていますが、未だ普及しているとは言い難いです。当施設でもPOEM導入について、ESDの延長で行いたいと指導医から相談がありましたが、私自身が見学したことしかないため行えず、申し訳ない気持ちでした。同じ治療であっても、日本で推奨されている前壁切開と欧米で主流な後壁切開の違い7–9や、治療後の有害事象であるバレット粘膜10などの比較データは整理する必要がありそうです。北米でのPOEMの需要は高く、今後習得したいと感じました。その他、消化管領域では食道術後狭窄へのRIC (radial incision and cutting)や、薬剤抵抗GERDへのARMAなどといった治療も数回ながら経験できました。
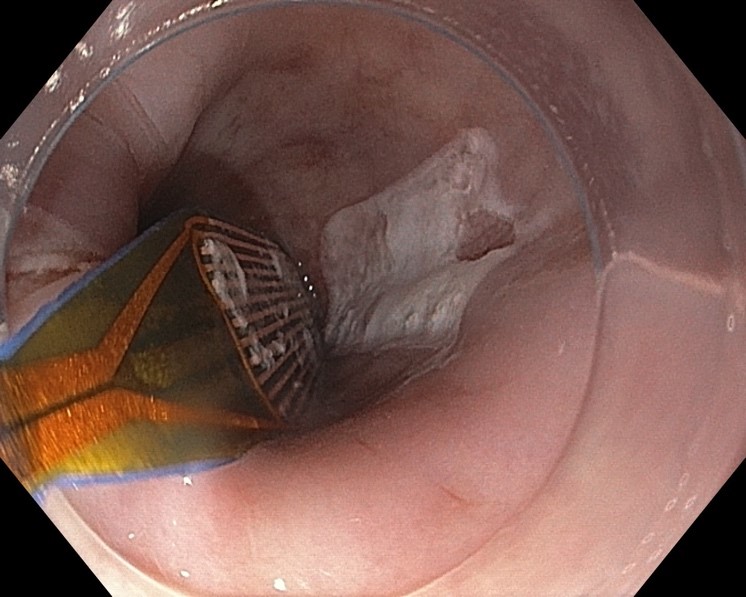
バレット食道へのラジオ波焼灼
4. まとめ
北米ではこのような内視鏡治療に特化した育成プログラムがあり、フェロープログラムを完遂すれば独り立ちと、明確になっています。日本ではどの段階で独り立ちか曖昧な印象があり、標準化されたプログラムの経験は勉強になりました。また、臨床スキルだけでなく、医師としての自信や自立心が決められた期間で身に付くこともプログラムのメリットと言えます。上級医の指導は毎年のプログラムを通して洗練されており、指導を請いながらその指導法を学ぶこともできます。言語や風習の違いなど戸惑うことは日常茶飯事ですが、それらを直に触れることも留学の醍醐味と言えます。カナダの問題として、治療内視鏡フェローの修練を積めるのは毎年十数人であり、消化器レジデント修了者が毎年百人程度いて、海外からも応募があることを考えると熾烈な競争になります。高い専門性と質を担保したり、医療の偏在性を避けることに繋がっていますが、自分が望んだ治療に全く携われないという状況が考えられない日本とは、大きな隔たりを感じました。
日本の内視鏡学は海外から敬意を払われており、先輩方が積み上げてこられた実績の大きさを実感しました。一方、グローバル化が進む中で海外の動向を理解したり、留学でしか得られないネットワークや刺激的な毎日を経験できたことは大変貴重に感じました。今回の寄稿で、「治療内視鏡プログラムがあるなんて知らなかった」や「留学のイメージが湧いた」と感じる方がいたら嬉しいです。留学してこの技術を得ようという決意を持った人であれば、日本と北米のハイブリッド研修はとても意義があると思います。
留学に際し温かく送り出して下さった福田勝之先生をはじめ、聖路加国際病院の先生方に感謝いたします。また、留学中にDr. Robert (カナダ、クイーンズ大学)、Dr. Yen・Dr. Barkun (カナダ、マギル大学)、Dr. Khashab・Dr. Ngamruengphong(米、ジョンズホプキンス大学)、Dr. Kalloo (米、マイモナイズメディカルセンター)、深見悟生先生 (米、メイヨークリニック)、相原弘之先生 (米、ハーバード大学)、西村誠先生 (米、スローンケタリングがんセンター)のもとを訪問させていただき、見聞を広める機会もいただけましたことに厚く御礼申し上げます。留学を志す方の参考になれば幸いです。

治療内視鏡チームでの宴

同僚の先生方
5. 文献
- Jagtap N, Kumar JK, Chavan R, et al. EUS versus MRCP to perform ERCP in patients with intermediate likelihood of choledocholithiasis: a randomised controlled trial. Gut. 2022.
- Suzuki M, Sekino Y, Hosono K, et al. Endoscopic ultrasound versus magnetic resonance cholangiopancreatography for the diagnosis of computed tomography-negative common bile duct stone: Prospective randomized controlled trial. Digestive endoscopy : official journal of the Japan Gastroenterological Endoscopy Society. 2022; 34: 1052-9.
- Buxbaum JL, Abbas Fehmi SM, Sultan S, et al. ASGE guideline on the role of endoscopy in the evaluation and management of choledocholithiasis. Gastrointest Endosc. 2019; 89: 1075-105.e15.
- Wang Y, Wang RH, Ding Z, et al. Wet- versus dry-suction techniques for endoscopic ultrasound-guided fine-needle aspiration of solid lesions: a multicenter randomized controlled trial. Endoscopy. 2020; 52: 995-1003.
- Giannone F, Crippa S, Aleotti F, et al. Improving diagnostic accuracy and appropriate indications for surgery in pancreatic cystic neoplasms: the role of EUS. Gastrointest Endosc. 2022; 96: 648-56.e2.
- 6. Marino A, Bessissow A, Miller C, et al. Modified endoscopic ultrasound-guided double-balloon-occluded gastroenterostomy bypass (M-EPASS): a pilot study. Endoscopy. 2022; 54: 170-2.
- Fukuda H, Sato H, Fujiyoshi Y, et al. Risks of refractory chest pain after peroral endoscopic myotomy in achalasia-related esophageal motility disorders: short-term results from a multicenter study in Japan. Gastrointest Endosc. 2022; 96: 620-9.e4.
- Jing W, Luo X, Yang J, Wu J, Chen Y, Deng K. An Updated Meta-analysis: Similar Clinical Efficacy of Anterior and Posterior Approaches in Peroral Endoscopic Myotomy (POEM) for Achalasia. Gastroenterology research and practice. 2022; 2022: 8357588.
- Ichkhanian Y, Abimansour JP, Pioche M, et al. Outcomes of anterior versus posterior peroral endoscopic myotomy 2 years post-procedure: prospective follow-up results from a randomized clinical trial. Endoscopy. 2021; 53: 462-8.
- Vespa E, Pellegatta G, Chandrasekar VT, et al. Long-term outcomes of peroral endoscopic myotomy for achalasia: a systematic review and meta-analysis. Endoscopy. 2022.








