2025年06月06日体験記・寄稿
体験記:米国における内視鏡診療の現状と日本との比較

ニューヨーク州立大学ダウンステート
マイモナイズメディカルセンター
治療内視鏡医
白鳥 安利
はじめに
米国は移民の国と称されるような、多民族によって押し上げられてきた歴史的背景を持ちます。医療の現場においても人の流動性が高く、さまざまな国籍の医師が医療チームに加わり、各々の専門性を活かしています。各国の技術を取り入れ、機器開発を組み合わせることで、治療成績の向上を目指しています。
私は日本で消化管および胆膵内視鏡を経験し、カナダでの治療内視鏡フェローを経て、2023年に渡米しました。日本で培ったESDなどの技術が必要とされる一方で、米国独自のアプローチ法や新たなデバイスを経験しています。日本が世界をリードしている内視鏡分野ですが、米国にも独自の発展過程があり、将来性を感じています。本稿が米国における内視鏡診療の現状をお伝えするとともに、国際的な知見や多角的な視点を深め、日本の内視鏡診療のさらなる発展に貢献できましたら幸いです。
1. 米国の卒後研修、消化器診療を取り巻く環境
米国では、内科レジデント3年および消化器フェロー3年を修了した後、アテンディング(指導医)として働きます。消化器フェローは内科フェロープログラムの中で最も人気が高く、応募者のうち実際に消化器科へのキャリアに進めるのは60-65%にとどまります1。この人気の背景には、疾患の多様性や豊富な専門領域、内視鏡という手技の習得が挙げられます1。また、米国では女性の消化器医の割合が高く、消化器フェローの34%、肝臓フェローの46%に相当します1 (日本は14%, 2022年内視鏡専門医データ)。フェロー期間には、外来、コンサルテーション、上下部内視鏡、抄読会、学会発表などを通じて、消化器診療の基礎を体系的に学びます。さらに治療内視鏡のサブスペシャリティを取得する場合は、アドバンスフェロープログラムを1〜2年追加することが求められます。この枠も米国全体で年間約96名に限られており2、フェロー修了者の総数(約520名)や海外からの応募を含めると、熾烈な競争になります。このように、米国では希望する診療科や治療領域に携われないことも珍しくありません。高い専門性や質の確保、医療偏在の是正を目的とした制度ですが、日本のように希望する診療分野を自分で選択できる制度は、非常に恵まれていると感じます。私自身は米国でフェローを経験していませんが、現地の後輩から相談を受ける中で、この競争の厳しさを実感しています。
また、病棟業務体系も日米間で大きな違いがあります。米国ではレジデントとホスピタリストが病棟を担当し、消化器科はコンサルテーションを受け、助言を行う立場です。点滴や看護師への具体的な指示は、すべてホスピタリストが担います。結果として、内視鏡医が処置に専念しやすい環境が整えられています。
さらに、米国ではナースプラクティショナーやフィジシャンアシスタントといった専門職が充実しています。問診、外来・処置の予約、大腸内視鏡の前処置処方など、日本では医師が行う業務の多くがサポートされており、これらの分業体制は業務効率化に大きく寄与しています。
2. 治療内視鏡医の役割
米国では、早朝から始まるカンファレンスに加え、7時台には1件目の予定治療を開始することが一般的です。緊急内視鏡の件数も多く、たとえばESDが数件予定されている午前枠に緊急ERCPをこなさなければならないなど、日中の業務は非常に多忙です。Tumor boardやM&Mカンファレンスでは、症例の解説や外科医・腫瘍内科医への提言が求められます。米国の治療内視鏡医は、多くの施設において上下部EMR、ESD、POEM、バレット食道アブレーション、PEG/PEJ、EUS、ERCP、消化管ステント、内視鏡的縫縮など、幅広い手技を担当します。近年では、機能性疾患や肥満症への内視鏡介入も注目を集めています。消化管と胆膵を分ける文化はなく、幅広いスキルを有することが高く評価されます。そのため、日本の大学病院のように専門臓器に特化するスタイルとは異なります。これらの手技はアドバンスフェロー期間中に一通り経験することができますが、技術的な習熟はアテンディングとなった後にさらに高めていくことになります。
米国は国民性が多様であるとともに、各内視鏡医が受けてきたトレーニング背景も多岐にわたるため、同じ疾患に対しても選択される治療に違いが見られます。そのため、個人の技量に依存せず、汎用性の高い手技やデバイスが受け入れられやすい傾向にあります。現時点では、ESDは一部の施設に集中していますが、POEMに精通した医師がESDトレーニングを開始すると、トンネル法の応用により習得が早まる傾向にあります。
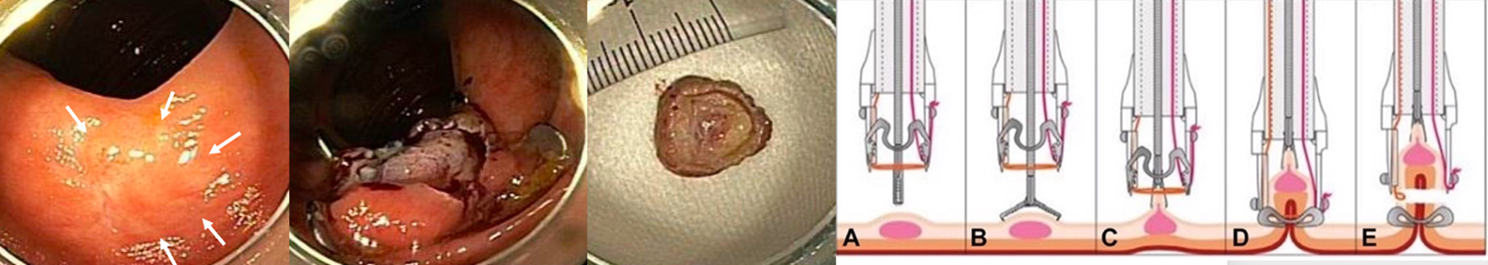
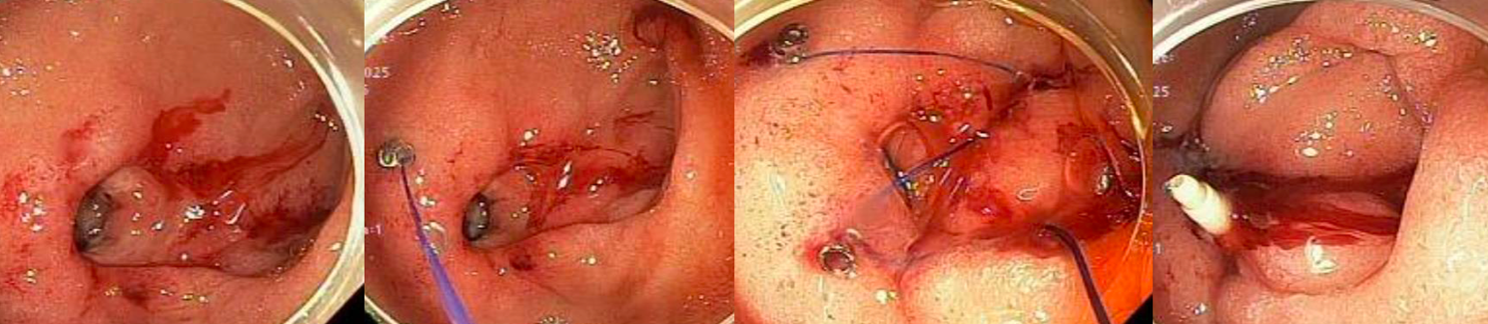
米国では産学連携が進んでおり、技術的な課題をデバイス開発で克服しようというアイデアが生まれやすいです。たとえば、大腸EMR後再発に対して、日本では難易度が高いながらもESD が選択される一方で、米国ではFTRD(消化管全層切除デバイス)による全層切除が選択されます。FTRDによる切除は処置時間が10分程度と短く、簡便です。比較的小さい消化管粘膜下腫瘍(15mm未満)にも使用されます。また、日本でさまざまな縫縮法が考案されるのに対し、米国では専用の縫縮デバイス(OverStitchやX-Tack)が普及しているため、新たな縫縮法が議論の中心となることはありません。食道バレット病変に対する背景粘膜の焼灼治療(ラジオ波や凍結療法)も米国では一般的であり、これらの機器は年々進化を続けています。今後、このようなデバイスは日本でも導入される可能性があります。
米国では、すべての内視鏡処置の鎮静および全身麻酔を麻酔科医が担当するため、鎮静度が管理され、内視鏡医は手技に専念できます。一方、呼吸や心機能評価などにより麻酔科の判断で治療が延期されることも珍しくありません。また、深い鎮静下では大腸内視鏡時の体位変換がしづらいという課題もあります。
治療内視鏡医に限らず、米国の医師は患者を獲得する努力が求められます。患者は主にかかりつけ医から「担当医宛」に紹介されるため、紹介が得られなければ、日中の業務がない状況も起こり得ます。この点は、日本のように「診療科」に患者が来院し、曜日ごとに担当医が割り当てられる体制とは大きく異なります。米国では、自由競争の中で実力を発揮することが求められており、それが医師の研鑽や医療の質の向上につながっています。病院にとって紹介患者の獲得は重要であり、多くの医師がこの体制を健全な競争と捉えています。また、出来高制の診療報酬制度は日々の診療に影響しており、医師は勤務中に手を抜くことなく、コンサルトや内視鏡に積極的に対応する印象があります。治療内視鏡分野では、ERCPなどの胆膵治療には手厚い診療点数が設定されているのに対し、ESDは依然として点数化の対象外となっています。
3. 治療内視鏡領域における教育
米国における教育とは、アテンディングによるフェローへの指導を意味します。アテンディングはその年次に関わらず同等の裁量権が与えられますが、フェローが行うすべての医療行為の責任を負います。フェロー教育は重要な業務の一つとされ、定期的に双方向によるフィードバックが行われるのが特徴的です。フェローはEUSやERCPを年間約300件ずつこなしながら、食道アブレーションやPOEMなどの消化管治療も習得していきます。たとえばEUSでは、TEESATというチェックリストに基づく抜き打ち評価を行い、トレイニーがinstructionを要さずに各臓器を描出できるかなど、ASGE(米国消化器内視鏡学会)が推奨する到達度目標が運用されています。
ESDの指導は施設ごとに多様ですが、胃癌罹患率が低い米国では、日本で行われる傾向がある胃前庭部などの難易度が低い部位から始め、直腸、結腸へステップアップさせる段階が踏みにくい実情があります。そのため、大腸EMR、tip-in EMR、直腸ハイブリッドESDを経て、純粋な大腸ESDへと段階的に難易度を上げるなど、形を変えた教育法が行われています。

4. 機能性疾患
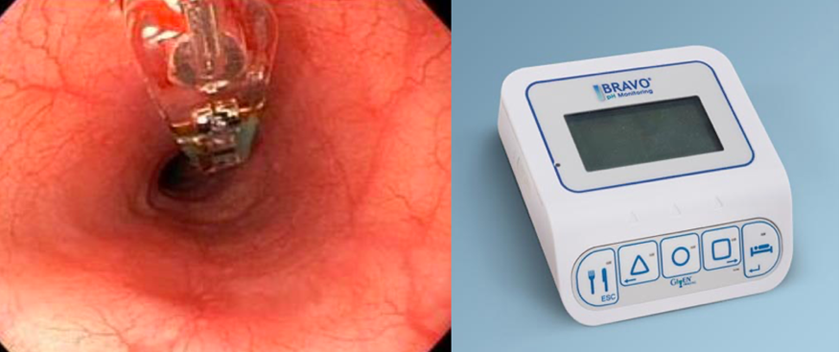
GI mortilityやneurogastroenterologyと称される消化管機能性分野は、米国で大きく発展しています。全てのフェローはローテーションを通じてこの分野を学ぶため、mortility専門医はどの病院でも欠かせません。対象疾患はGERD、アカラシア、びまん性食道痙攣、好酸球性食道炎、胃不全麻痺、便秘、慢性腸閉塞、過敏性腸症候群など多岐にわたり、提供される検査には、高解像度食道内圧検査、pHモニンタリング、Bravo(カプセル型pHモニタリング)、胃排出シンチグラフィー、高解像度肛門内圧検査、SmartPillなどがあります。これらの検査が充実しているため、胃不全麻痺(gastroparesis)の診断が容易で、治療としてG-POEMが施行されます。日本で機能性ディスペプシア(FD)とされる患者の中には、実際にはこの器質的疾患の可能性があると感じています。
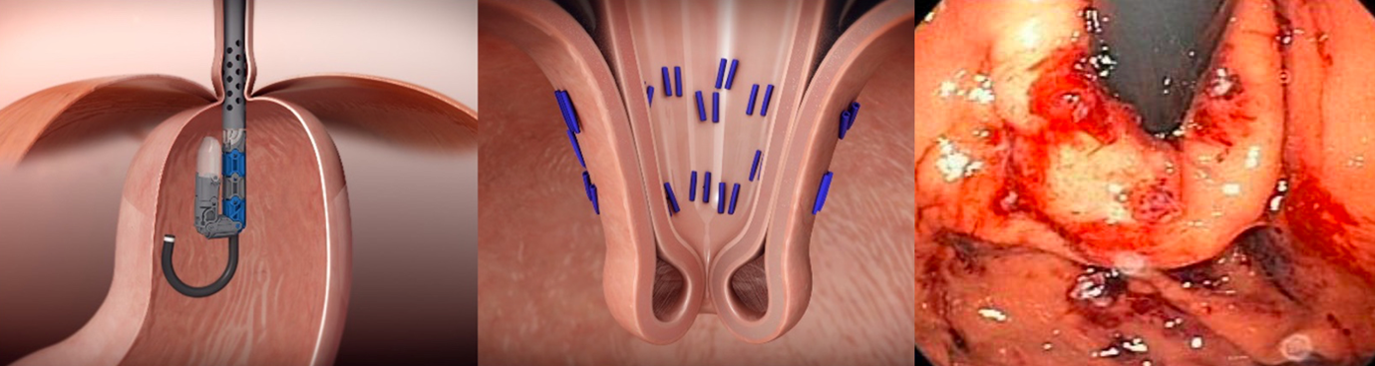
Mortility専門医が行う治療としては、バルーン拡張術、ボトックス注射、Stretta(ラジオ波によるGERD治療)、TIF(経口的無切開噴門形成術)などがあります。TIFは食道胃接合部のvalve機能を高める役割があり、高い成功率に加えPPI離脱率もARMAやARM-Pより高い報告があります3,4.
また、motility医師は治療内視鏡医と連携し、POEM時のEndoFlipでの周術期評価や、Hirshsprung病の確定診断に必要な直腸全層生検なども行います。E-POEMは日本で開発されましたが、派生したZ-POEM(食道憩室)やG-POEMはむしろ米国からの報告5が多くなっており、豚検体を用いたZ-POEMやG-POEMのハンズオントレーニングも各地で充実しています。
5. 食道分野 (バレット食道/腺癌)
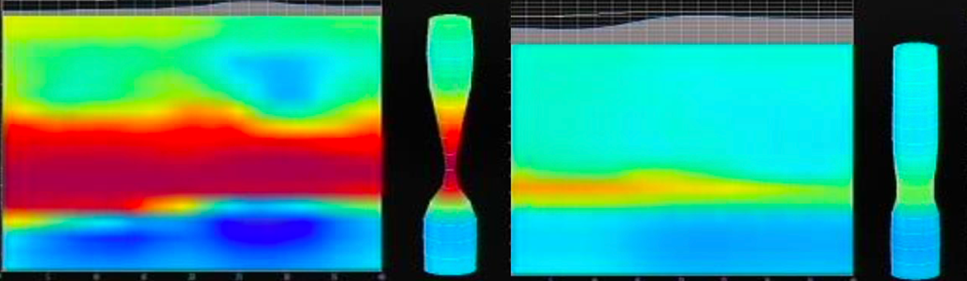
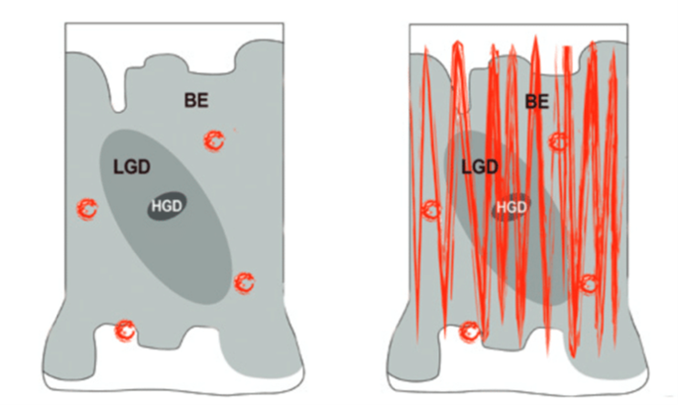
バレット粘膜に対して、Seattleプロトコルに基づいたランダム生検が米国では行われてきましたが、WATS(Wide Area Transepithelial Sampling)の併用がdysplasia検出の感度を高めるとされています6。WATSはブラシを愛護的に擦過し、より広範囲かつサンプリングエラーの少ない細胞採取を可能としています。High-grade dysplasiaあるいは粘膜内癌で、2cm以上やbulkyな病変にはESDを行うことがASGEより推奨されています。バレット病変に対するESDは、GERDやRFA後など背景粘膜の炎症がある状態で実施しなければならず、日本の扁平上皮癌に対するESDとは解剖学的違いに加えて、線維化の状況も異なります。Dysplasia切除後には、残存するバレット粘膜に対してRFAまたはCryotherapyによる根治治療が行われます。
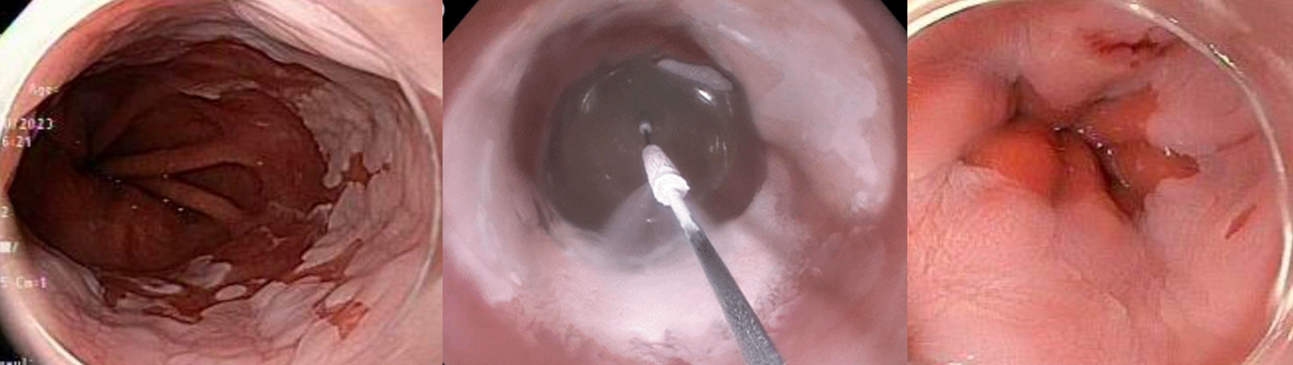
6. 胃癌診療
胃癌に対する診断・治療は日本が世界をリードしています。ご存知のとおり、日本では1980年代から、早期発見・治療を目的とした胃癌検診制度が整備され、これが基盤となり、その後の画像診断(NBIなどの画像強調、拡大、AI導入など)、読影会、ESD治療へと発展しました。一方、米国では胃癌の罹患率が低く(全がんの第15位、2023年NIH)、これまで検診体制はおろか、大きな課題として取り上げられてきませんでした。しかし実際には、ニューヨーク州やカリフォルニア州など、特にアジア系や東欧系住民の多い地域では、胃癌が多く認められています7。こうした背景を受け、米国でも日本をはじめとするアジア諸国の取り組みを参考にすべきとの議論が挙がっています。今後、米国では質の高い胃内視鏡検査の普及が必要であり、そのうえでハイリスク地域や患者に焦点を当てた検診制度の導入が求められます。
胃内視鏡検診は日本と韓国で導入されていますが、その有効性に関して、日本が韓国に劣るという報告がGastroenterology誌からあります8。日本では胃癌検診の参加率が低く(日本28%、韓国56%)、さらにX線検診への依存度が高い(内視鏡検査の割合:日本19%、韓国72%)ため9⁻10、精度管理の面で課題を抱えています。今後の超高齢化社会という時代背景も踏まえ、日本の胃癌検診の動向は米国からも注目が集まっています。
胃ESDについては、米国の多くの施設において切除後は可能な限り内視鏡的縫縮を行い、日帰り治療とするのが特徴的です。これは、高額な入院費を避けるニーズが高いことに加え、縫縮デバイスの普及により後出血や穿孔などのリスクを可能な限り低減できること、かかりつけ医や紹介元の消化器医によるフォロー体制が整っていること、さらにPPIは1回40mgを1日2回投与が一般的など、日本とは異なる医療体制が関係しています。
7. 大腸癌診療
米国では大腸がんの罹患率および死亡率が高く(全がんの中で第4位、2024年NIH)、その予防や検診に対する社会的関心が高いです。特に、便潜血検査(FIT)よりも精度の高い便中DNA検査(Cologuard)が、Medicareを含む多くの保険でカバーされており、広く市民に普及しています。また、内視鏡検査を含む大腸がん検診は、米国で45歳の時点で保険によって無償で受診でき、このタイミングで検査を受けようとする意識が高いのが特徴的です。さらに、adenoma detection rate(ADR)を基準とした質的評価が重視されており、十分な観察時間やフード、反転操作による襞裏観察といった工夫も積極的に取り入れられています。結果として、検診受診率は80%と非常に高く(日本は48%、国民生活基礎調査)、大腸がんによる死亡率は年々大きく低下しております(米国7.9 vs. 日本11.3 /10万人、2022年WHO)。その取り組みとその成果において、米国は日本よりも優れていると言えます。
一方、米国で大腸ESDを行う際には、日本と異なる課題に直面します。EMR後再発や不適切な点墨による線維化、肥満患者における大きな呼吸性変動、160cmと長く取り回しの難しい下部消化管スコープ、4Lの前処置による液体貯留など、手技の難易度を高める要因があります。トレーニングの機会は各セミナー等を通じて豊富に存在しますが、治療前の段階で回避可能である上記困難例(不必要な生検・EMR・点墨、不正確な所見)11を減らすことが、今後の課題です。なお、EMR後再発に関しては、10〜15mm程度までは、先述のFTRDでの全層切除が可能で、選択肢として一定の役割を果たしています。
8. 胆膵内視鏡
米国におけるEUSの敷居は低く、胆管炎が疑われる症例や、CTで原因が明確でない膵炎に対して、MRCPより優先されます。各治療内視鏡医はアドバンスフェロー修了時に少なくとも300件のEUSを経験しており、その診断感度・特異度はMRCPを上回るとされています12。EUS後にERCPが必要と判断された場合には、移動式Cアームを用いて、同一セッションでERCPを施行することが可能で、透視室への患者移動を省略できる利点もあります。ERCPのカニュレーションは、短いガイドワイヤーを用いて術者自身が操作するphysician-controlled wire-guided cannulation(WGC)が標準的です。
膵嚢胞性病変に対する穿刺吸引検査は、米国で日常的に行われており、日本で懸念されている播種のリスクは、極めて低いとする結論が得られています。現在では、実施の有無について議論されることはなく、外科医やかかりつけ消化器医から積極的に求められます。穿刺液は細胞診に加えて遺伝子解析が実施され、特にPancreGENという遺伝子解析キットの普及と、その大規模なサンプル解析13は、米国における遺伝子診断技術の充実性を反映しています。
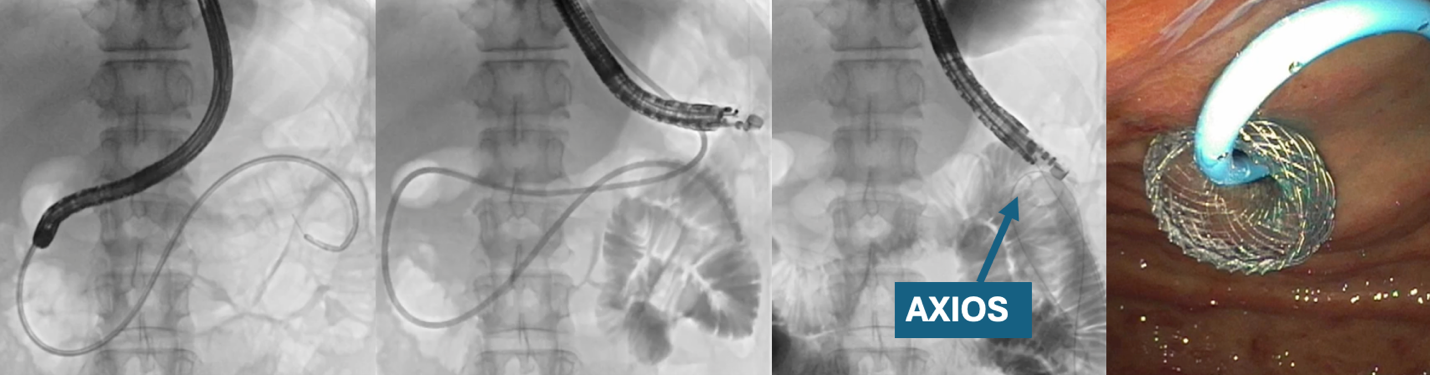
HOT-AXIOS(lumen-apposing metal stent)は、米国において適応範囲が広く、膵被包化壊死をはじめ、経十二指腸的胆嚢・胆道ドレナージ、Roux-en-Y再建後腸管に対するEDGE(EUS-directed transgastric ERCP)、さらには胃空腸バイパス(G-Jステント)など、さまざまな場面で使用されています。Roux-en-Y再建術は、米国では肥満手術として日常的に行われており、EDGEや腹腔鏡補助下ERCP(laparoscopic-guided ERCP)の技術を習得していることが、理想とされます。また悪性胃十二指腸狭窄(gastric outlet obstruction, GOO)に対しては、日本ではステント留置が第一選択とされていますが、米国ではG-Jステントの選択肢もあるため、どちらを選択するか症例ごとに議論される傾向があります。近年では、標的となる空腸を確実に緊満・描出するためのシステムが開発されており、今後さらにG-Jステントの普及が進むと考えられます。
おわりに
このように、日米の内視鏡診療を比較すると、さまざまな興味深い相違点が浮かび上がってきます。「日本の内視鏡診断・治療は優れている」といった一面的な評価だけでは不十分であり、臓器や疾患領域によっても異なります。今回詳述できませんでしたが、米国では肥満内視鏡治療や、エンドヘパトロジー(EUS下での門脈圧測定や胃静脈瘤治療)と称される肝臓への内視鏡的介入も盛んであり、実臨床において重要な役割を果たしています。
現地での診療を通じて、私は院内外の多くの医師と連携する機会に恵まれました。温かく迎えていただき、不安は安心へ、そして期待へと変わっていきました。渡米前に抱いていた米国内視鏡診療に対する印象も、より前向きなものとなっています。最後に、米国での内視鏡診療に際し、多くの助言をいただきました深見悟生先生、西村誠先生、相原弘之先生、富澤裕先生、ならびに日々支えてくださっている当院内視鏡スタッフに心より感謝申し上げます。本稿が米国における内視鏡診療の実情をお伝えする一助となれば幸いです。

参考文献
- Starkey M, Daboul J, Lang J, et al. Trends in female representation in gastroenterology fellowships in the United States. Ann Gastroenterol 2022;35:577-583.
- Qayed E, Sheth SG, Aihara H, et al. Advanced endoscopy fellowship training in the United States: recent trends in ASGE advanced endoscopy fellowship match, trainee experience, and postfellowship employment. Gastrointest Endosc 2021;93:1207-1214.e2.
- McCarty TR, Itidiare M, Njei B, Rustagi T. Efficacy of transoral incisionless fundoplication for refractory gastroesophageal reflux disease: a systematic review and meta-analysis. Endoscopy 2018; 50(7): 708-25.
- Garg R, Mohammed A, Singh A, et al. Anti-reflux mucosectomy for refractory gastroesophageal reflux disease: a systematic review and meta-analysis. Endosc Int Open 2022; 10(6): E854-e64.
- Zhang LY, Canto MI, Schweitzer MA, et al. Gastric per-oral endoscopic myotomy (G-POEM) for the treatment of gastric sleeve stenosis: a feasibility and safety study. Endoscopy 2022;54:376-381.
- Gross SA, Smith MS, Kaul V US Collaborative WATS3D Study Group. Increased detection of Barrett’s esophagus and esophageal dysplasia with adjunctive use of wide-area transepithelial sample with three-dimensional computer-assisted analysis. United European Gastroenterol J. 2018;6:529–535.
- Pittman M, Avleen K, Shiratori Y, et al. Assessing Gastric Cancer Risk Among Immigrant Populations in Brooklyn: A Call for Targeted Screening Programs. Clin Gastroenterol Hepatol 2024 publish in press.
- Sun D, Mülder DT, Li Y, et al. The Effect of Nationwide Organized Cancer Screening Programs on Gastric Cancer Mortality: A Synthetic Control Study. Gastroenterology 2024;166:503-514.
- Shiratori Y, Ishii N, Kalloo A. Disparities in Gastric Cancer Screening: A Comparative Analysis of Japan and South Korea. Gastroenterology 2024;167:815-816.
- Ishii N, Shiratori Y, Ishikane M, et al. Population effectiveness of endoscopy screening for mortality reduction in gastric cancer. DEN Open 2024;4:e296.
- Ichkhanian Y, Lahr RE, Guardiola JJ, Rex DK. Frequency of errors in colorectal lesion description and management prior to referral to a tertiary center. Gastrointest Endosc. 2024.
- Jagtap N, Kumar JK, Chavan R, et al. EUS versus MRCP to perform ERCP in patients with intermediate likelihood of choledocholithiasis: a randomised controlled trial. Gut. 2022.
- Paniccia A, Polanco PM, Boone BA, et al. Prospective, Multi-Institutional, Real-Time Next-Generation Sequencing of Pancreatic Cyst Fluid Reveals Diverse Genomic Alterations That Improve the Clinical Management of Pancreatic Cysts. Gastroenterology 2023;164:117-133.e7.








